Estados Unidos: Pfizer solicita uso de emergencia para su vacuna en niños entre 12 y 15 años
La farmacéutica busca ampliar el rango de edad de su fórmula, la que demostró ser segura en los adolescentes en los ensayos clínicos.
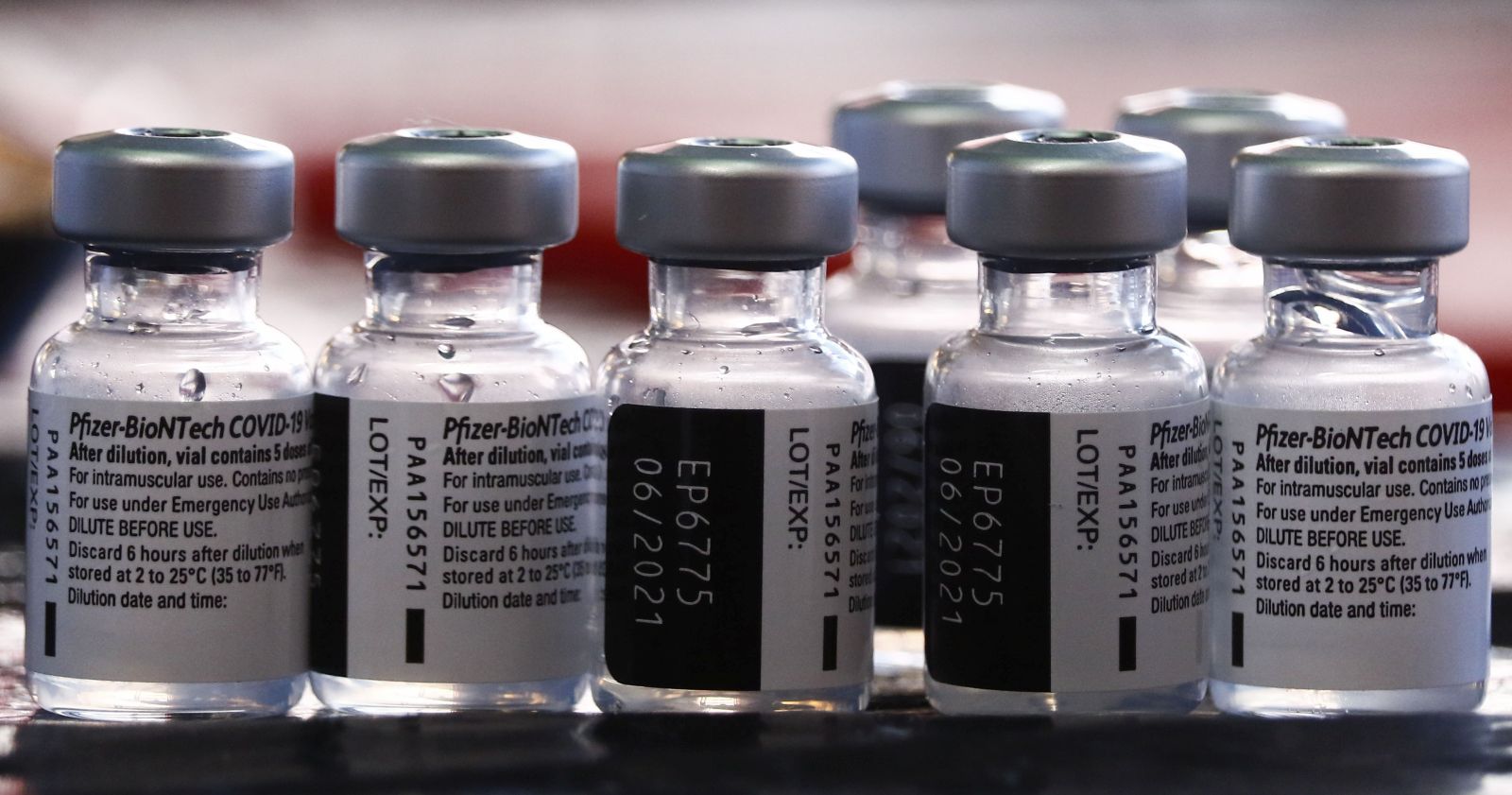 Hasta ahora la vacuna está autorizada para personas hasta los 16 años. AGENCIA UNO/ARCHIVO.
Hasta ahora la vacuna está autorizada para personas hasta los 16 años. AGENCIA UNO/ARCHIVO.
La farmacéutica Pfizer presentó durante este viernes ante la Administración de Alimentos y Medicamentos (FDA, por su sigla en inglés) una autorización para el uso de emergencia de la vacuna contra el COVID-19 para niños y adolescentes de entre 12 y 15 años.
Según lo informado por NBC, la compañía -que desarrolló la fórmula junto con la empresa de biotecnología alemana BioNTech-, presentó los antecedentes de sus ensayos clínicos de fase III, que demostraron seguridad y 100% de efectividad en personas de este rango etario, en estudios que aún están a la espera de la revisión de los pares.
Albert Bourla, director de Pfizer, señaló que la vacunación en niños comenzaría antes del inicio del próximo año escolar, lo que ayudaría para retomar las actividades en las escuelas.
Buddy Creech, experto en enfermedades infecciosas pediátricas del Centro Médico de la Universidad de Vanderbilt en Nashville, Tennessee, añadió que “al extender los grupos de edad que pueden recibir la vacuna, podemos continuar nuestros esfuerzos para proteger a los más vulnerables: adultos mayores, así como adultos y adolescentes con afecciones médicas subyacentes”.
Hasta el momento la vacuna de Pfizer y BioNTech está autorizada desde los 16 años en adelante tanto en Estados Unidos como en Chile.














