ISP aprobó el uso de la vacuna Janssen de Johnson & Johnson
El organismo dio luz verde a la fórmula contra el COVID-19, que requiere de una sola dosis para entregar la protección necesaria contra la enfermedad.
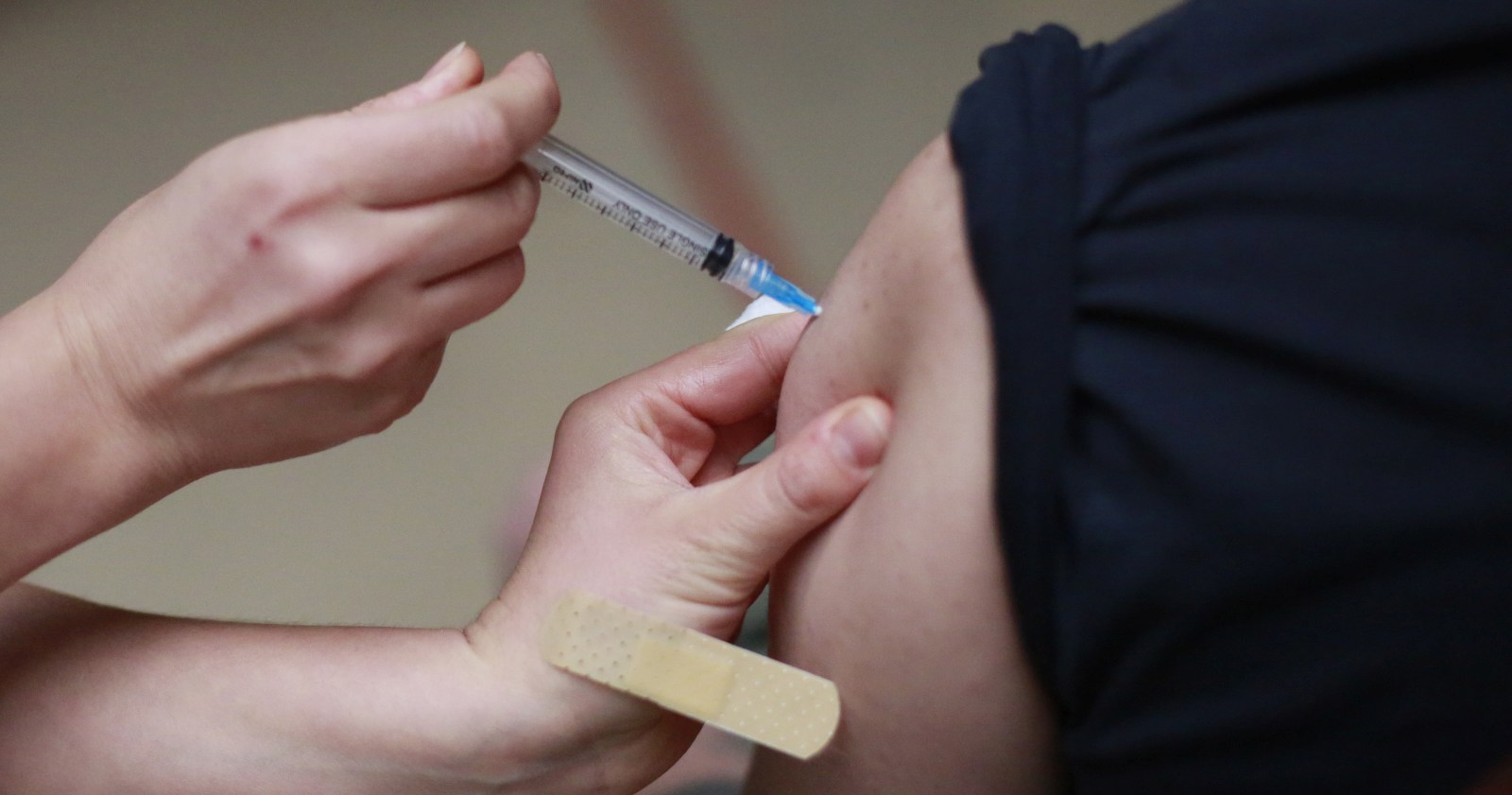 La fórmula contra el COVID-19 se transformó en la quinta en recibir la autorización en el país. AGENCIA UNO/ARCHIVO
La fórmula contra el COVID-19 se transformó en la quinta en recibir la autorización en el país. AGENCIA UNO/ARCHIVO
El Instituto de Salud Pública (ISP) aprobó el uso de emergencia de la vacuna contra el COVID-19 desarrollada por el laboratorio belga Janssen, subsidiario de la gigante farmacéutica estadounidense Johnson & Johnson.
Se trata de la quinta fórmula autorizada en el país tras Pfizer/BioNTech, CoronaVac de Sinovac, AstraZeneca y CanSino. Además, se trata del segundo fármaco disponible que requiere de una sola dosis para entregar la protección necesaria contra la enfermedad.
La entidad reguladora nacional homologó los antecedentes usados por la Organización Mundial de la Salud (OMS), que dio luz verde para el ingreso del suero a la plataforma de distribución de vacunas Covax al mostrar datos concretos sobre su calidad, seguridad y eficacia.
Esta vacuna está autorizada para su uso en la población en Brasil, Reino Unido, Canadá, Colombia, Unión Europea, México y Estados Unidos, en personas de 18 años y más.
Heriberto García, director (s) del ISP, estuvo a cargo de la reunión de expertos del departamento Agencia Nacional de Medicamentos (ANAMED), donde consideraron los antecedentes de Covax para revisar la inoculación con Janssen de Johnson & Johnson.
“Entre diciembre de 2020 y abril de 2021, el ISP autorizó cuatro vacunas para uso de emergencia en Chile, la primera es la vacuna del Laboratorio Pfizer, posteriormente la vacuna Coronavac de Sinovac, luego AstraZeneca y Cansino. Todas estas vacunas, fueron evaluadas y sometidas a la opinión de expertos en Chile. En el caso de Janssen, se validó un proceso que llevó adelante la máxima entidad de salud a nivel mundial, la OMS, que, además, es el organismo que otorga las acreditaciones a las Agencias Reguladoras de Medicamentos, como el ISP”, señaló el directivo.
García agregó que a través de esta homologación con la OMS se podrán evaluar otras vacunas que no han llegado al país como la de Moderna y la china Sinopharm, que también recibieron la aprobación de Covax.
La fórmula monodosis fue desarrollada bajo la tecnología de adenovirus de tipo 26 recombinante. En personas por sobre los 18 años, incluidos adultos mayores de 60 años, demostró ser eficaz en un 66,9%, después de los 14 días. En casos severo/crítico, después de 14 días de vacunación, la eficacia fue de un 76,7%, y 28 días después de la vacunación, fue de 85,4%.