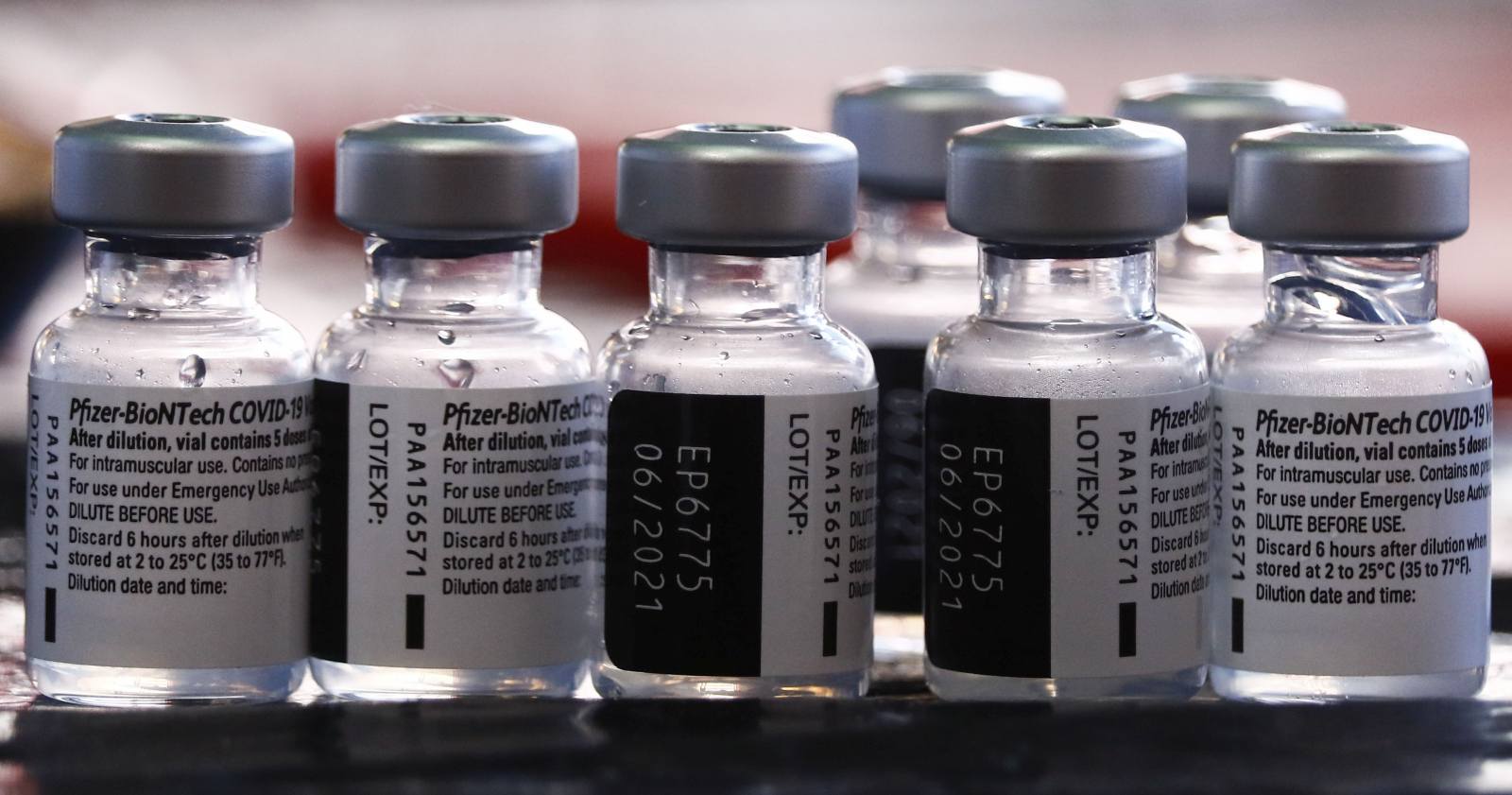
El Instituto de Salud Pública (ISP) recibió una solicitud de la farmacéutica estadounidense Pfizer, donde se busca autorizar en Chile el uso de emergencia de la vacuna contra el COVID-19 en niños de entre 12 y 16 años.
La compañía presentó los antecedentes luego que la Administración de Medicamentos y Alimentos de Estados Unidos (FDA, por su sigla en inglés) aprobara su aplicación en menores de edad al verificar su eficacia y seguridad.
“Ellos presentan esto y lo que tenemos que revisar es si las dosis son las adecuadas, si se presentaron efectos adversos distintos a los del estudio clínico original y todo lo que eso implica. La buena noticia es que teniendo la aprobación de la FDA, es una aprobación que no requiere comité de expertos, sino que una mirada técnica si es que se cumple o no con lo que se presentó en el estudio clínico. Esperamos tener respuesta la próxima semana, entre lunes y miércoles”, señaló el director (s) del ISP, Heriberto García, a La Tercera.
El directivo del organismo regulador afirmó que además de solicitar la vacunación en niños, la farmacéutica Pfizer pedirá que “la temperatura de almacenamiento por 30 días sea de 2º a 8º grados (celsius)”, lo que permitirá tener las dosis por mayor tiempo en los vacunatorios.